- Speisewasser
Speisewasser (feed-water; eau d'alimentation; aqua d'alimentazione) zur Wasserversorgung der Dampfkessel.
Über Art und Verunreinigung des S., Kesselsteinbildung, Ablagerung des Kesselsteins und Einfluß des Kesselsteins auf die Wirtschaftlichkeit sowie über Verhütung der Bildung des Kesselsteins s. Kesselstein.
Über Einrichtungen zur Abscheidung des Kesselsteins aus dem S. – entweder im Dampfraum, im Wasserraum oder auch außerhalb des Kessels – s. Kesselsteinabscheider.
S. muß beim Eintritt in den Kessel möglichst warm sein. Warmes S. vermindert Wärmeschwankungen im Dampfkessel. Es werden ungünstige Materialbeanspruchungen vermieden und Kohlen erspart. Daher Vorwärmung erwünscht. Über Anlagen zur Vorwärmung des S.s. Speisewasservorwärmung.
S. muß rein und weich, d.h. möglichst frei von mechanischen und chemischen Verunreinigungen sein. Schädliche Stoffe werden beseitigt durch Reinigung und Enthärtung.
Reinigung von Schlamm, Lehm, Abfällen, Öl u.s.w. Schwere Beimengungen läßt man in Klärbehältern sich absetzen. Für leichtere Stoffe erfolgt die mechanische Reinigung durch Filter. Die Größe des Filters ist derart zu bemessen, daß die Wassergeschwindigkeit höchstens 1·2 mm für 1 Sekunde beträgt. Als Material des Filters empfiehlt sich am besten Kies und zerkleinerter Koks in mehreren Schichten mit 1/2–3 mm Korngröße. Die Filter sind häufig durch Umrühren und Auswaschen zu reinigen. Für geringen Raumbedarf und große Leistung kommen Schnellfilter mit mehreren übereinanderliegenden, auf je einem Siebboden gelagerten Quarzsandschichten in Verwendung.
Öle und Fette sind aus dem S. durch Ölabscheider und Filter zu entfernen. Schon ein Zusatz von 0·005–0·01 g im l ist bedenklich. Das Filtermaterial besteht hierbei aus Koks, Holzwolle, Sägespänen oder Schwamm.
Bei erheblichem Eisengehalt ist Reinigung erforderlich, da sich unlösliches Eisenoxyd bildet, das Kessel und Rohre verschlammt. Das Wasser wird in Enteisenungsanlagen durchlüftet und gefiltert. Über neuere Anlagen s. Guillery, Neuere Wasserversorgungsanlagen.
Die Enthärtung des S. erfolgt, um Kesselsteinbildner, insbesondere Kalk- und Magnesiasalze, unschädlich zu machen. Die wichtigsten Kesselsteinbildner sind die Sulfate und Karbonate von Kalzium und Magnesium. Kesselstein entsteht dadurch, daß durch Wärmesteigerung bzw. Verdampfen des Wassers die Löslichkeit der im Wasser gelösten Verbindungen sich verringert und die unlöslich gewordenen Mengen sich in festem Zustand ausscheiden.
Für die Beurteilung eines S. kommt nicht ausschließlich die Menge der Kesselsteinbildner in Frage, sondern auch der Gesamtgehalt an gelösten Stoffen, der als Abdampfrückstand bezeichnet wird. Auch die bei starkem Eindampfen gelöst bleibenden Salze wirken schädlich, da sie durch Siedeverzug Spucken, d.i. Wasserauswurf aus dem Rauchfang der Lokomotive verursachen. Stark salzhaltige S. führen zu Korrosionen der Kesselbleche.
Nach den vom preußischen Ministerium der öffentlichen Arbeiten herausgegebenen Grundzügen für die Errichtung von Bahnwasserwerken und Vorschriften für die Wasseruntersuchung ist S. als gut anzusehen, wenn in 1 l klarem Wasser der Verdampfungsrückstand nicht mehr als 100–200 mg beträgt. Wasser mit einem Verdampfungsrückstand von 200 bis 300 mg ist ziemlich gut, mit einem solchen von 300–500 mg noch eben brauchbar. Wasser mit mehr als 500 mg Verdampfungsrückstand auf 1 l muß chemisch gereinigt werden. Der Zusatz ist nach dem Ergebnis einer chemischen Untersuchung zu bemessen.
Außer nach den Verdampfungsrückständen wird die Güte des S. auch nach Härtegraden gemessen. Ein deutscher Härtegrad = 1 Gewichtsteil Kalk auf 100.000 Gewichtsteile Rohwasser (1 deutscher Härtegrad = 1·25 englischem = 1·79 französischem Härtegrad). Die Gesamthärte des S. ist die Summe der Gewichtsteile an Kalk und der auf Kalk umgerechneten Gewichtsteile Magnesia. Dabei entspricht 1 Gewichtsteil Magnesia 1·4 Gewichtsteilen Kalk.
S. von 10–15 deutschen Härtegraden gilt im allgemeinen noch als weich. Die Enthärtung des S. ist für leicht zu reinigende Kessel notwendig und nutzbringend, wenn die Härte mehr als 12 deutsche Härtegrade beträgt, wogegen bei schwer befahrbaren Kesseln, also auch Lokomotivkesseln, schon 6–7 deutsche Härtegrade die äußerste Grenze bilden, bis zu der ungereinigtes Wasser ohne wesentlichen Nachteil verwendet werden kann.
Bestimmung der Härte. Sie erfolgt am genauesten durch Errechnung aus der durch die chemische Untersuchung des S. ermittelten Zusammensetzung. Ungenauer wird sie durch Titrieren mit einer Seifenlösung bis zur bleibenden Schaumbildung nach dem Schütteln bestimmt. Die zum Titrieren benutzte Seifenlösung wird auf ein Wasser von bekannter Härte oder auf eine Chlorbariumlösung von bekanntem Gehalt eingestellt. Man unterscheidet Gesamthärte, bleibende Härte und vorübergehende Härte. Bleibende Härte ist der nach längerem Kochen verbleibende Rest an Härte. Sie wird im wesentlichen durch den Gehalt des S. an schwefelsaurem Kalk (Gips) und schwefelsaurer Magnesia bedingt. Die Abnahme der Härte, vorübergehende Härte, wird durch den Gehalt an saurem kohlensauren Kalk bzw. Magnesia verursacht, die beim Kochen unter Verlust an Kohlensäure sich als unlösliche kohlensaure Salze abscheiden.
Ein Wasser von hoher bleibender Härte bei gleicher Gesamthärte ist schlechter als ein solches von niedrigerer bleibender Härte, da der sich ausscheidende Kesselstein infolge seines höheren Gehalts an Gips (schwefelsaurem Kalk) wesentlich härter und schwerer abklopfbar ist.
Bei der Enthärtung werden die Kesselsteinbildner chemisch in unlösliche Kalk- und Magnesiaverbindungen umgesetzt. Die festen Teile, die sich dabei bilden, werden auf mechanischem Wege entfernt.
Nach den Zusätzen, die dem S. beigegeben werden, unterscheidet man Enthärtung durch: 1. Kalk, 2. Soda, 3. Kalk und Soda, 4. Ätznatron, 5. Bariumhydroxyd, 6. Bariumkarbonat und 7. Permutit.
1. Bei der Enthärtung durch Kalk wird Kalkwasser (Lösung von gebranntem Kalk) dem zu reinigenden S. hinzugesetzt. Aus dem im Wasser gelösten sauren kohlensauren Kalk entsteht unlöslicher einfach kohlensaurer Kalk.
Ca(HCO3)2 + Ca(OH)2 = 2CaCO3 + 2H2O
Mg(HCO3)2 + Ca(OH)2 = MgCO3 + CaCO3 + H2O
Die Ausfällung der kohlensauren Magnesia ist unvollständig. Auf a g des in der Analyse angegebenen kohlensauren Kalks sind 0·56 a g gebrannter Kalk erforderlich. Wasser, das freie Kohlensäure enthält, erfordert eine größere Menge gebrannten Kalks, als die vorgenannte Rechnung ergibt.
2. Bei der Enthärtung durch Soda (kohlen saures Natron) wird der schwefelsaure Kalk in kohlensauren Kalk umgewandelt.
CaSO4 + Na2CO3 = CaCO3 + Na2SO4.
Die Umwandlung erfordert längere Zeit, die der schwefelsauren Magnesia ist unvollständig. Auf b g schwefelsauren Kalk sind 106/136 b g = 0·78 b g wasserfreie Soda (Ammoniaksoda) erforderlich.
3. Die Enthärtung durch gleichzeitigen Zusatz von Kalk und Soda wird am häufigsten angewendet und ist am meisten zu empfehlen. Berechnung der Zusätze wie oben unter 1 und 2.
4. Die Enthärtung durch Ätznatron zielt auf Entfernung des schwefelsauren Kalks und Verringerung des sauren kohlensauren Kalks hin.
Auf a g schwefelsauren Kalk sind 0·6 a g Ätznatron (Natriumhydroxyd) erforderlich, außerdem wird der Gehalt des Wassers an doppeltkohlensaurem Kalk um 1·5 a g vermindert.
5. Bariumhydroxyd wirkt in ähnlicher Weise durch Bindung der Kohlensäure. Außerdem wird die im Gips enthaltene Schwefelsäure als unlöslicher schwefelsaurer Baryt entfernt.
Auf a g CaSO4 sind erforderlich 2·3 a g kristallisiertes Bariumhydroxyd. Außerdem werden von dem im Wasser gelösten doppeltkohlensauren Kalk noch 1·5 ag als kohlensaurer Kalk ausgefällt.
6. Bariumkarbonat wirkt nur, wenn es künstlich gefällt ist. Gemahlenes natürliches Bariumkarbonat (Witherit) ist wirkungslos. Auf a g schwefelsauren Kalk sind 1·45 a g Bariumkarbonat erforderlich. Zweckmäßig wird diese Enthärtung mit der Enthärtung durch Kalk (vgl. 1 der Aufzählung) verbunden.
7. Permutit ist ein durch Zusammenschmelzen von Feldspat, Kaolin, Sand und Soda erhaltenes, dem in der Natur vorkommenden Zeolith ähnliches Produkt, das die Eigenschaft hat, Kalksalze in Natriumsalze umzuwandeln. Das über Permutit langsam filtrierte Wasser enthält an Stelle des sauren kohlensauren Kalks Natriumbikarbonat. Die Permutitfilter werden mit der Zeit unwirksam, lassen sich aber durch Behandlung mit Chlornatriumlösung wieder wirksam machen.
Die Zusätze können dem Wasser beigegeben werden, bevor es in den Kessel gelangt oder im Kessel selbst. Das letztere Verfahren ist nicht zu empfehlen, da die bei der Enthärtung sich bildenden Rückstände im Kessel verbleiben und diesen verunreinigen.
Für die Enthärtung außerhalb des Kessels sind besondere Vorrichtungen erforderlich, die für die Verfahren zu 1–6 (s.o.) keine grundsätzlichen Unterschiede aufweisen.
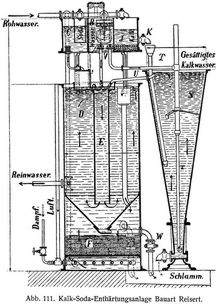
Die als Beispiel dargestellte Kalk-Soda-Enthärtungsanlage von Reisert, Köln (s. Abb. 111), besteht aus dem Kalksättiger S, dem Klärbehälter D, dem darüber angeordneten Verteilungsbehälter und dem Kiesfilter F. Letzterer ist bei Platzmangel in den Klärbehälter eingebaut. Die in dem Raum J des Verteilungsbehälters bereitete Kalkmilch wird durch den Hahn K und das darunter befindliche Rohr unten in den Kalksättiger eingeführt. Durch das Ventil V und das Rohr T fließt aus dem Raum B eine bestimmte, dem Ergebnis der chemischen Untersuchung entsprechende Wassermenge unter die Kalkmilch und wirbelt diese in die Höhe. Bei dem nach oben zunehmenden Querschnitt des Sättigers wird die Geschwindigkeit des aufsteigenden Wassers ständig geringer. Die Kalkteilchen fallen daher wieder zurück. Das gesättigte Kalkwasser gelangt durch das Rohr U in das Mischrohr E des Klärbehälters. Hierhin fließt auch aus dem Raum C des Verteilungsbehälters die genau bemessene Menge der Sodalösung und aus dem Raum B das Rohwasser. Die ausgefällten Kesselsteinbildner setzen sich in dem Klärbehälter als Schlamm ab, der von Zeit zu Zeit durch den Hahn W abgelassen wird. Das Wasser steigt aus dem Mischrohr E in dem Behälter D in die Höhe, fließt durch ein Überfallrohr in das Kiesfilter F und verläßt durch ein Ventil die Enthärtungsanlage.
Zur Reinigung des Filters wird mit einem Ejektor Luft durch das Filter gedrückt.
Über die verschiedenen Bauarten und über Einzelheiten der Vorrichtungen s. Wehrenfennig, Über die Untersuchung und das Weichmachen des Kesselspeisewassers.
Die Klärbehälter werden entweder oben offen (vgl. Abb. 111) oder geschlossen ausgeführt. Bei den geschlossenen Behältern kann das Wasser mit nur einer Pumpe durch die Enthärtungsanlage in den Wasserturm gedrückt werden. Für offene Behälter sind 2 Pumpen, eine für Rohwasser, die zweite für das enthärtete Wasser, erforderlich. Zudem bedingt die offene Anlage noch einen Zwischenbehälter, aus dem das enthärtete Wasser gepumpt wird. Offene Bauart ist zu empfehlen, wenn für das Wasser, etwa wegen starken Eisengehalts, Durchlüftung erwünscht ist. Bei geschlossener Bauart ist Durchlüftung nur durch Druckluft herzustellen. Die Zusätze können hierbei dem Rohwasser nur durch genau eingestellte Hähne und Ventile zugeführt werden. Bei offenen Behältern ist Zuleitung der Lösung durch Heberleitung, Schöpfwerk oder Kippschale erforderlich.
Die Klärbehälter müssen möglichst groß sein, da für die Nachreaktion, die nach der ersten Ausfällung der Kesselsteinbildner stattfindet, eine geraume Zeit – wenigstens 3 Stunden – erforderlich ist.
Auf dem üblichen kalten Wege läßt sich mit obigen Vorrichtungen die Enthärtung bis auf etwa 5 deutsche Härtegrade erreichen. Bei starker Vorwärmung des Rohwassers ist eine Enthärtung bis auf etwa 2 Härtegrade erzielbar.
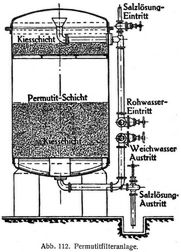
Eine noch weitere Enthärtung erfolgt bei Permutitbehandlung des Wassers. Eine Filteranlage hierfür – in geschlossener Ausführung – ist in Abb. 112 dargestellt.
Das Rohwasser fließt von einem oberen Behälter dem Filter zu, durchströmt die Permutitschicht und wird in enthärtetem Zustand in einen hochstehenden Reinwasserbehälter gedrückt. Zur Erhaltung der Wirksamkeit der Anlage wird in den Betriebspausen eine Kochsalzlösung in das Filter geleitet.
Literatur: Hütte, 22. Aufl., Bd. II, S. 57 f. – Heidepriem, Die Reinigung des Kesselspeisewassers. – Wehrenfennig, Über die Untersuchung und das Weichmachen des Kesselspeisewassers; Bahnhofsanlagen, Reinigung des Speisewassers. Eis. T.d.G. – Stockert, Handbuch des Eisenbahnmaschinenwesens, Wasserspeisung von Schäfer. Berlin 1908, Julius Springer. – Guillery, Das Maschinenwesen der preußisch-hessischen Staatseisenbahnen, neuere Wasserversorgungsanlagen.
http://www.zeno.org/Roell-1912. 1912–1923.